- 聯(lián)系我們
- 電話:13241188166
- 座機:010-56216670
-

掃一掃,添加微信
保健食品備案原料目錄“納新”在即,數(shù)十種排隊入場,100+未來可期!
2025-08-14

近年來,保健食品原料備案目錄的動態(tài)調整持續(xù)引發(fā)行業(yè)關注,成為驅動行業(yè)規(guī)范發(fā)展與創(chuàng)新升級的關鍵風向標。目前,由24種營養(yǎng)素補充劑與10種功能原料構成的“24+10”格局已形成。與此同時,原料擴容的步伐不斷加快:30余種復方配伍試點原料已進入實踐探索階段,另有數(shù)十種原料處于研究推進過程中,未來總量有望突破100種。這一系列進展標志著我國保健食品原料管理體系正從“基礎保障”向“多元拓展”跨越,逐步構建起更完善、更多元、更適配公眾健康需求的全新框架,為行業(yè)高質量發(fā)展注入持續(xù)動力。
(一)營養(yǎng)素補充劑(24種)
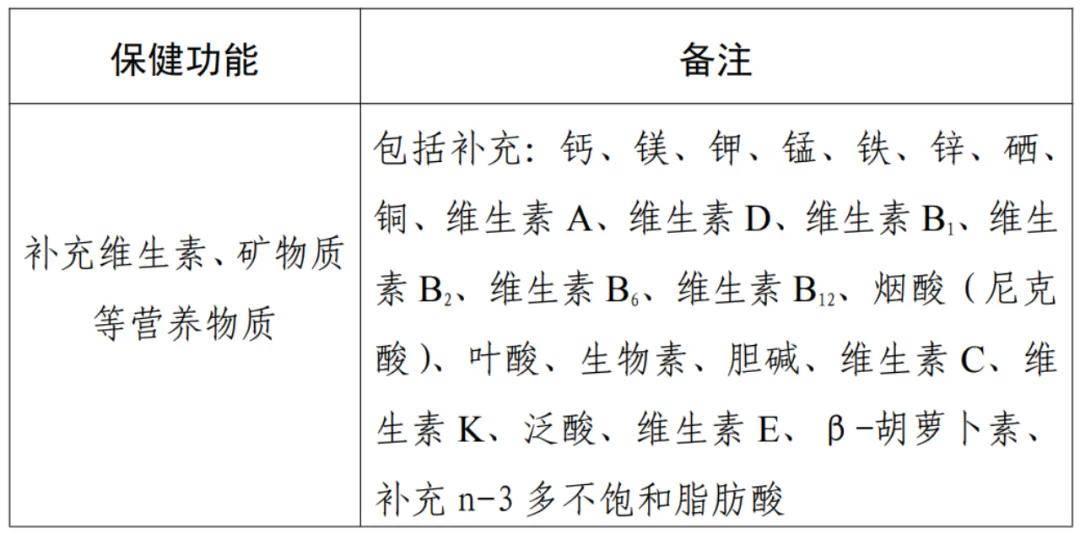
依據(jù)《保健食品原料目錄 營養(yǎng)素補充劑(2023年版)》,24種營養(yǎng)素及對應的85個化合物被明確納入,功能聲稱嚴格限定于補充特定營養(yǎng)素,為基礎營養(yǎng)補充類產(chǎn)品搭建了標準化合規(guī)框架。其中,“酪蛋白磷酸肽+鈣”作為復配原料創(chuàng)新納入,通過促進鈣吸收的協(xié)同作用優(yōu)化補鈣產(chǎn)品備案路徑;DHA藻油則支持單方或復配備案,以“補充n-3多不飽和脂肪酸”的功能覆蓋全人群需求,豐富了產(chǎn)品形態(tài)。
(二)功能原料(10種)
功能原料的納入呈現(xiàn)分階段推進特征,精準對接市場需求:
2021年3月,輔酶Q10、破壁靈芝孢子粉、螺旋藻、魚油、褪黑素5種原料首批落地,以成熟的功效研究數(shù)據(jù)開啟功能原料備案先河;
2023年10月,大豆分離蛋白、乳清蛋白加入,填補了優(yōu)質蛋白補充類原料的備案空白;
2024年5月,人參、西洋參、靈芝正式納入,要求原料品種嚴格遵循《中國藥典》標準且僅限單方使用。其中,人參、西洋參可聲稱“有助于增強免疫力”和“緩解體力疲勞”,靈芝則聚焦“增強免疫力”,實現(xiàn)了傳統(tǒng)養(yǎng)生資源與現(xiàn)代監(jiān)管標準的有機融合。
國家市場監(jiān)督管理總局(含原國家食品藥品監(jiān)督管理總局)通過兩次專項課題招標,累計推動63種(類)原料研究,成為原料目錄擴充的重要推動力。
(一)2017年首次招標(26種系列原料)
2017年9月,針對沙棘(油)、人參(紅參)、西洋參、天麻等26種原料啟動研究。成果顯著:輔酶Q10等5種納入首批功能原料;人參、西洋參、靈芝也于2024年納入;天麻、三七等8種進入復方配伍試點名單。>>點擊查看<<
(二)2018年第二批招標(37類原料)
2018年9月,分6個包組推進阿膠、蜂膠、松花粉、DHA、益生菌等37類原料研究。轉化成果包括:DHA藻油、大豆分離蛋白等4種納入目錄;黃精、薏苡仁等8種進入復方配伍試點,為藥食同源原料的復方應用開辟路徑。>>點擊查看<<
目前,多領域原料的納入進程正處于關鍵推進階段:
復方配伍試點深化:2025年5月,市場監(jiān)管總局特殊食品司組織貴州、廣東、廣西等8個省(區(qū))召開座談會,研究先行先試開展保健食品復方配伍備案,初選30余種中藥材為復方產(chǎn)品備案探路,加速傳統(tǒng)配方的現(xiàn)代化轉化。
特色原料落地提速:2023年7月,市場監(jiān)管總局在人大建議答復中提及正推動番茄紅素、蜂膠等納入目錄;同年8月,中國農(nóng)業(yè)科學院蜜蜂研究所承擔的“蜂膠、蜂王漿納入備案目錄”項目通過驗收。2025年6月,市場監(jiān)管總局披露正研制《保健食品原料 鹽酸氨基葡萄糖》等13種原料質量標準,計劃將氨糖、硫酸軟骨素納入目錄。
益生菌與益生元拓展:2025年7月,菊粉、低聚果糖、抗性糊精納入備案目錄論證啟動會召開,計劃10月底前完成論證,進入實質性階段;8月,市場監(jiān)管總局明確推進9種益生菌(如動物雙歧桿菌乳亞種Bb-12等)安全性評價,擬納入目錄支持備案管理。
此外,更多原料處于研究評估中,100+原料陣容未來可期。
從“24+10”的現(xiàn)有格局到“100+”的近景藍圖,保健食品原料備案目錄的更新不僅是數(shù)量的跨越,更是監(jiān)管邏輯、產(chǎn)業(yè)創(chuàng)新與公眾健康需求的深度融合。這一進程既通過標準化降低企業(yè)合規(guī)成本,激發(fā)中小企業(yè)創(chuàng)新活力,又以科學驗證筑牢安全防線。展望未來,隨著更多原料的規(guī)范化納入,我國保健食品行業(yè)將將實現(xiàn)從“數(shù)量增長”到“質量提升”的跨越,構建以精準營養(yǎng)為核心的健康產(chǎn)業(yè)生態(tài),為健康中國提供堅實支撐。
北京中健天行醫(yī)藥專注于營養(yǎng)保健食品領域的技術研發(fā)、注冊申報及成果轉化,擁有一站式研發(fā)創(chuàng)新服務平臺,保健食品SC證品牌生產(chǎn)基地,中國保健食品批文轉讓交易平臺,建立了一站式產(chǎn)學研協(xié)作技術創(chuàng)新和服務體系,獲ISO9001國際質量體系認證,致力于為企業(yè)提供高標準研發(fā)創(chuàng)新申報服務,歡迎申報企業(yè)來電與我們咨詢交流!